Målriktad genmodifiering för djurpatogena klamydia
Forskare vid Umeå universitet, i samarbete med forskare vid University of Maryland och Duke University, USA, har för första gången genomfört målinriktad genmodifiering i djurpatogena bakterien Chlamydia caviae.
Publicerad: 2019-11-08 Uppdaterad: 2023-06-13, 15:47 Text: Eva-Maria Diehl
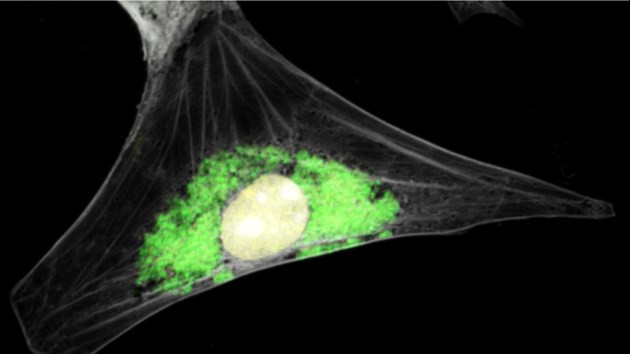
Marsvin cell smittad med klamydia bakterien Chlamydia caviae (vit färgad är cellen, cellkärnan är gul färgad klamydia bakterier är grön färgade)
BildBarbara SixtKlamydia är den vanligaste sexuellt överförda bakteriella sjukdomen i världen. Sjukdomen orsakas av bakterien Chlamydia trachomatis. Det beräknas att mer än 100 miljoner människor varje år smittas av klamydia, och smittan är ofta en orsak till infertilitet. Chlamydia trachomatis är också ansvarig för ögoninfektioner och är den vanligaste smittsamma orsaken till blindhet i några delar av världen.
Det är känt att klamydia inte bara påverkar människor utan även djur. När bakterien smittar kor, får, grisar eller kycklingar, kan infektionerna orsaka betydande ekonomisk skada. Men även sällskapsdjur, som katter, marsvin och papegojor kan smittas av klamydia. Vissa djurpatogena klamydia skiljer sig biologiskt från den för människan mycket smittsama Chlamydia trachomatis. Forskarna har visat att vissa djurpatogena smittoämnen också överförs till människor. Dessa så kallade zoonoser kan utvecklas till allvarliga infektioner och ibland vara livshotande.
Nu publicerar MIMS-forskare tillsammans med forskare från University of Maryland Baltimore och Duke University, USA, i tidskriften PLOS ONE en studie om hur de använde en ny metod för att undersöka virulensfaktorer i zoonotisk klamydia.
- För att förstå varför vissa klamydier kan orsaka infektioner hos människor och andra inte, måste vi undersöka hur dessa olika bakteriearter skiljer sig i deras förmåga att interagera med sina värdar, säger infektionsbiologen Barbara Sixt, en av projektledarna vid The Laboratory for Molecular Infection Medicine Sweden, MIMS, vid Umeå universitet.
Alla kända klamydier är intracellulära bakterier, vilket innebär att bakterierna invaderar mänskliga celler eller djurceller och replikerar sig inuti värdcellen. För att förändra värdcellen till ett perfekt hem för bakterierna producerar Chlamydia virulensfaktorer som påverkar cellens normala funktioner.
Intressant är att olika Chlamydia-arter bildar speciella uppsättningar av dessa faktorer.
- Det är möjligt att närvaron eller frånvaron av olika virulensfaktorer under infektionprocessen med olika Chlamydia-arter kan bestämma över deras förmåga att infektera olika värdar och deras förmåga att orsaka olika sjukdomar i dessa värdar, säger Barbara Sixt.
Vår förmåga att testa funktionen och betydelsen av specifika virulensfaktorer beror på experimentella strategier som gör det möjligt för forskare att skapa mutationer av bakterierna som sedan kan undersökas vidare i laboratoriet.
Medan sådana strategier nyligen har utvecklats för den mänskliga patogenen Chlamydia trachomatis, hade liknande experiment hittills inte genomförts i zoonotisk klamydia.
- Med hjälp av en metod som möjliggör att införa ett DNA-fragment på en specifik position i bakteriegenomet lyckades vi generera två mutanter av Chlamydia caviae, som saknar speciella virulensfaktorer", säger Kimberly Filcek, första författaren till studie.
- Detta visar att metoden som nyligen utvecklades i Chlamydia trachomatis kan tillämpas också på andra Chlamydia-arter.
Studiens författare fokuserade på Chlamydia caviae, en Chlamydia-art som främst infekterar marsvin, men som nyligen också visade sig att orsaka allvarliga lunginfektioner hos människor. Arten är också släkt med Chlamydia psittaci, en fågelpatogen som orsakar papegojsjuka i människor. Sjukdomen, är den vanligaste zoonotiska klamydiainfektionen som även förekommer i Sverige.

Forskare vid Umeå universitet som var delaktiga i studien om virulensfaktorer i zoonotiska bakterien Chlamydia caviae (från vänster Johan Henriksson, Katarina Vielfort, Barbara Sixt, Samada Muraleedharan)
BildKarsten MeierNu förändrade forskarna C. caviae två virulensfaktorer, IncA och SinC. En mutant utan IncA faktorn visade en förändrad struktur av den membranformiga vakuolen, inklusionskroppen, i värdcellen i vilken bakterierna tillväxer. Dessutom observerades att en SinC-mutant visade reducerad infektionsförmåga i kyckling-embryon, vilket tyder på att SinC bidrar till bakteriens förmåga att orsaka sjukdom hos djur. Intressant nog är SinC en faktor som endast produceras av zoonotisk klamydia, men inte av den huvudsakliga mänskliga patogenen C. trachomatis.
- I framtiden kommer vi att använda mutanten för att utforska molekylära infektionsmekanismer i SinC, förklarar Patrik Bavoil från University of Maryland.
- Även om det finns mycket kvar att lära sig om de båda virulensfaktorers funktion i C. caviae, kommer vårt senaste genombrott i genetisk modifiering av C. caviae att öppna nya spännande möjligheter att undersöka biologin för dessa patogener. Detta kan i framtiden potentiellt också möjliggöra alternativa sätt att behandla infektioner, avslutar Barbara Sixt.
Original publikation:
Kimberly Filcek, Katarina Vielfort, Samada Muraleedharan, Johan Henriksson, Raphael H. Valdivia, Patrik M. Bavoil, Barbara S. Sixt: Insertional mutagenesis in the zoonotic pathogen Chlamydia caviae. PLOS ONE, The Public Library of Science ONE, 07 November 2019
Read the publication in PLOS ONE:
https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0224324
Kontakt:
Barbara S Sixt, Assistant Professor
The Laboratory for Molecular Infection Medicine Sweden (MIMS)
Institutionen för molekylärbiologi
Umeå universitet, 90187 Umeå
barbara.sixt@umu.se, tel: +46 90-785 67 42
http://www.mims.umu.se/groups/barbara-sixt.html
Patrik M Bavoil, Professor
Department of Microbial Pathogenesis
University of Maryland, School of Dentistry
Baltimore, MD, USA
PBavoil@umaryland.edu, phone: +1 410 706 6789
https://www.dental.umaryland.edu/micropath/research/dr-patrik-bavoil-lab/







