Om den vetenskapliga studien
Studien har publicerats i den vetenskapliga tidskriften mBio och forskningen finansierades delvis av Vetenskapsrådet, Umeå centrum för mikrobiell forskning (UCMR), stressresponsmodelleringen vid IceLab Centre of Research Excellence, Kempestiftelserna och medicinska fakulteten vid Umeå universitet.
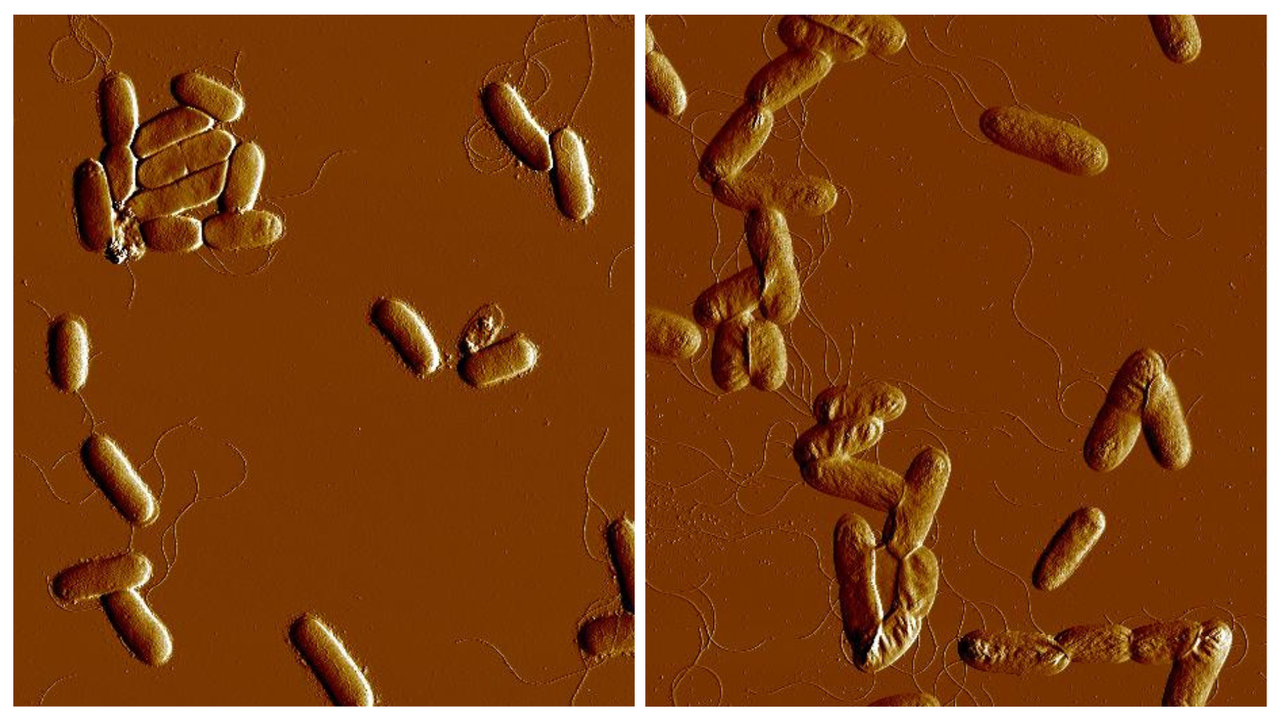
Waititu JK, Nilsson K, Larrouy-Maumus G, Costa TRD, Avican K.0.: RfaH is essential for virulence and adaptive responses in Yersinia pseudotuberculosis infection. mBio0:e02122-25.