
Bild: Chinnapong

Bild: Chinnapong
Forskningsprojekt Ungefär hälften av de som dör av prostatacancer dör trots att deras cancer upptäckts innan den har spridit sig och de därmed hade möjligheten att bli botade. Dagens behandlingar är tydligt otillräckliga för denna hög-risk grupp, men genom att introducera effektivare behandling redan i detta tidiga skede borde spridning kunna hindras och liv räddas. Effektivare behandlingar har ofta biverkningar, och då inte alla patienter drar nytta av dem, behövs säkra metoder att välja rätt behandling.
SPRINTR Swedish PRrecision medicine Initiative for Novel Treatment and Research syftar till att implementera optimerade molekylära, histologiska och imagebaserade metoder för precisionsmedicin och därmed öka överlevnaden bland män med hög-risk prostatacancer, samt minska onödiga biverkningar och kostnader för samhället. Projektet kommer även initiera ett arbetssätt kring kliniska studier, som genom samverkan av redan existerade infrastruktur för klinisk information med nationella register och databasresurser skapar en plattform för effektiv och öppen forskning.
BAKGRUND
Icke-metastaserad prostatacancer med hög risk är fortfarande en betydande orsak till dödlighet och de nuvarande behandlingsalternativen är otillräckliga. En stor andel av männen kommer att utveckla progression efter behandling med kurativt syfte. I detta skede, före kliniskt påvisbara metastaser, tror vi att intensifierad behandling skulle kunna öka överlevnaden.
Vid metastaserad prostatacancer har androgen deprivationsterapi följt av kemoterapi och nyare behandlingar inriktade på androgenreceptorvägen förbättrat överlevnaden. De är dock också förknippade med förhöjd toxicitet. Precisionsmedicin är nyckeln till att identifiera patienter som skulle kunna dra nytta av en upptrappning av behandlingen tidigare i sjukdomsförloppet.
Olika biomarkörpaneler, inklusive flytande biopsier och bilddiagnostik, har föreslagits för patientstratifiering. Denna studie kommer att etablera en precisionsmedicinsk plattform med fokus på molekylär profilering, avbildning och histologi för att förbättra överlevnadsgraden för högriskpatienter med prostatacancer. Vår plan innebär att vi analyserar retrospektiva kohorter för att identifiera biomarkörer, genomför en prospektiv klinisk multicenterstudie för att validera biomarkörsalgoritmer och vidare etablerar en biomarkörsdriven adaptiv randomiserad klinisk multicenterstudieplattform med flera armar. Dessutom kommer vi att inleda ett utvecklingsprogram för läkemedelsupptäckt baserat på målstyrda vägar som identifierats genom kontinuerlig profilering av försöksdeltagare med dålig respons på behandling.
MÅL
Att öka överlevnaden för patienter med lokalt avancerad högriskcancer genom att etablera en precisionsmedicinsk plattform baserad på molekylär profilering, bilddiagnostik och histologi.
Specifika mål är att:
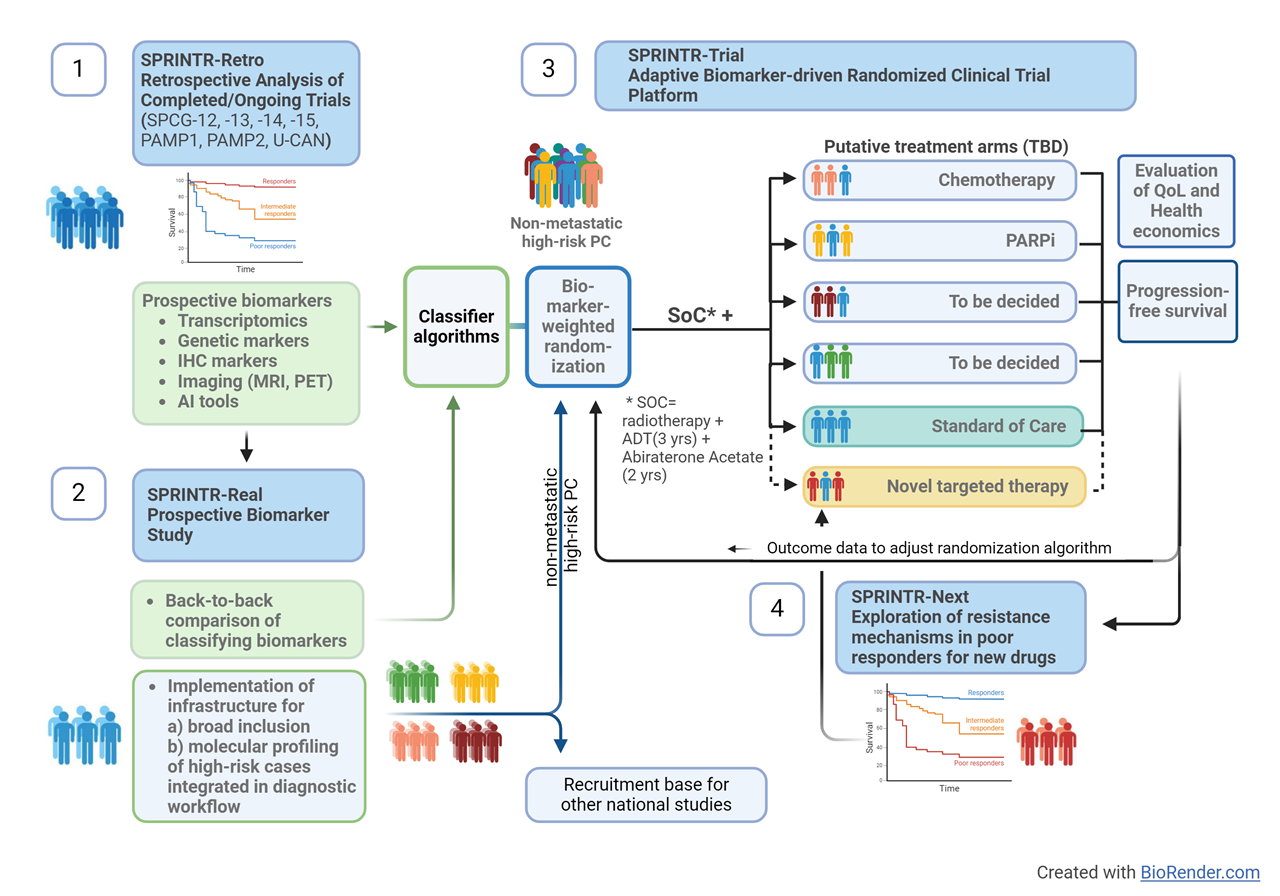
1. Utöka och slutföra pågående omfattande molekylär- och bildanalys av storskaliga retrospektiva kohorter för att utveckla beslutsalgoritmer för precisionsmedicin.
2. Starta en prospektiv icke-interventionell klinisk multicenterstudie för att validera och etablera biomarköralgoritmerna i en diagnostisk undersökning.
3. Omvandla den etablerade infrastrukturen från mål 2 till en biomarkörsdriven adaptiv multicenter, multi-arm randomiserad klinisk prövning (RCT) plattform med metastatisk fri överlevnad som primär slutpunkt. Biomarkörvägd randomisering kommer att stratifiera patienter till standardbehandling (SoC) eller behandlingsupptrappningsarmar såsom bildstyrd strålbehandling, tillägg av docetaxel, nya antiandrogener, PARP-hämmare, 177-Lu-PSMA radioligandterapi eller nya modaliteter som utvecklas under försöksperioden. Parametrar för livskvalitet (QoL) och hälsoekonomi kommer att integreras.
4. Initiera ett utvecklingsprogram för läkemedelsupptäckt baserat på målstyrda vägar som identifierats genom kontinuerlig transkriptomisk och genomisk profilering av försöksdeltagare
Sammantaget definieras projektets nyhet av dess fokus på högrisk PC före kliniskt manifesta metastaser, där tidigare inga biomarkörer har implementerats, och inkluderingen av inte bara genetiska utan även fenotypiska och bildbaserade biomarkörer jämfört med Probio- och STAMPEDE-studierna. Dessutom ökar inkluderingen av profileringsalgoritmer som härrör från metastaser potentialen att identifiera patienter med tumörer som är benägna att bilda metastaser.
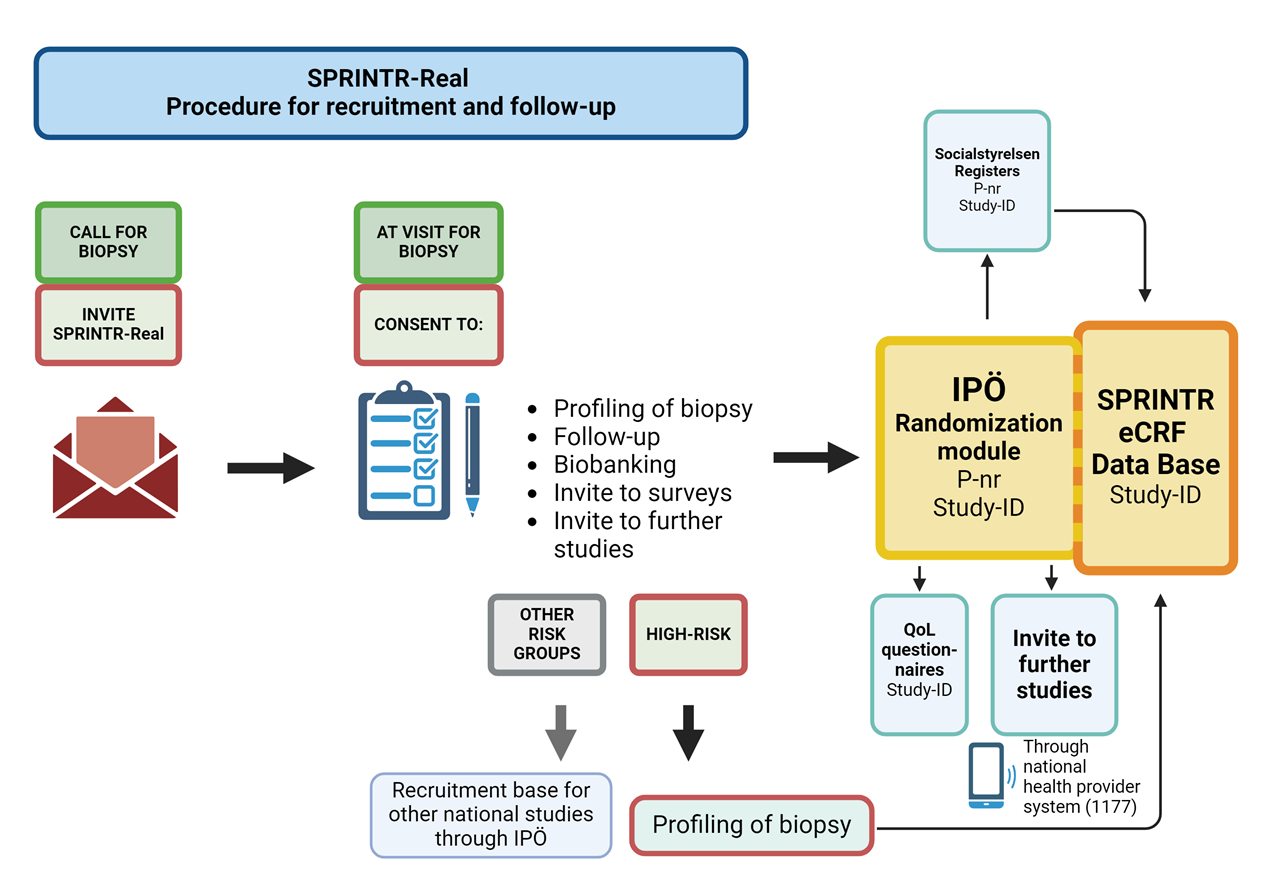
Ett annat mål med SPRINTR är att underlätta högkvalitativ forskning om prostatacancer i Sverige genom att integrera bred patientrekrytering och biomarkörprofilering i det diagnostiska flödet. Tillsammans med en automatisk uppföljningsfunktion för kliniska data från svenska register kommer detta att skapa en kontinuerligt växande forskningsdatabas som kan ligga till grund för patienturval och uppföljning i andra prostatacancerstudier i Sverige. SPRINTR kommer därmed att öka möjligheten till högkvalitativa, stora läkemedelsprövningar med effektiv rekrytering, minska den administrativa bördan för studiepersonal och möjliggöra god och jämlik tillgång till kliniska prövningar för patienter oavsett var i landet, eller av vilken läkare, de får sin behandling.
RELATERADE STUDIER
PUBLIKATIONER
Josefsson A, Effect of docetaxel added to bicalutamide in Hormone-Naïve non-metastatic prostate cancer with rising PSA, a randomized clinical trial (SPCG-14) https://pubmed.ncbi.nlm.nih.gov/37073813/
Spyratou V, Ki67 and prostate specific antigen are prognostic in metastatic hormone naïve prostate cancer https://pubmed.ncbi.nlm.nih.gov/37713321/
Sandgren K, Histopathology-validated lesion detection rates of clinically significant prostate cancer with mpMRI, [68Ga]PSMA-11-PET and [11C]Acetate-PET https://pubmed.ncbi.nlm.nih.gov/37615497/
Wikström P, Epithelial and Stromal Characteristics of Primary Tumors Predict the Bone Metastatic Subtype of Prostate Cancer and Patient Survival after Androgen-Deprivation Therapy https://pubmed.ncbi.nlm.nih.gov/37615497/
Thysell E, Clinical and biological relevance of the transcriptomic-based prostate cancer metastasis subtypes MetA-C https://pubmed.ncbi.nlm.nih.gov/34889043/
Järemo H, Investigating microRNA Profiles in Prostate Cancer Bone Metastases and Functional Effects of microRNA-23c and microRNA-4328 https://pubmed.ncbi.nlm.nih.gov/37173903/
Josefsson A, Circulating tumor cells mirror bone metastatic phenotype in prostate cancer https://pubmed.ncbi.nlm.nih.gov/30034626/
Josefsson A, Circulating Tumor Cells as a Marker for Progression-free Survival in Metastatic Castration-naïve Prostate Cancer https://pubmed.ncbi.nlm.nih.gov/28295408/
Gonora M, Characteristics of Patients in SPCG-15-A Randomized Trial Comparing Radical Prostatectomy with Primary Radiotherapy plus Androgen Deprivation Therapy in Men with Locally Advanced Prostate Cancer https://pubmed.ncbi.nlm.nih.gov/35813256/
Björklund J, The 90-day cause-specific mortality after radical prostatectomy: a nationwide population-based study https://pubmed.ncbi.nlm.nih.gov/34191407/
Schostak M, Practical Guidance on Establishing a Molecular Testing Pathway for Alterations in Homologous Recombination Repair Genes in Clinical Practice for Patients with Metastatic Prostate Cancer https://pubmed.ncbi.nlm.nih.gov/37714762/
Merseburger AS, Apalutamide plus androgen deprivation therapy in clinical subgroups of patients with metastatic castration-sensitive prostate cancer: A subgroup analysis of the randomised clinical TITAN study https://pubmed.ncbi.nlm.nih.gov/37708629/
Thysell E, Gene expression profiles define molecular subtypes of prostate cancer bone metastases with different outcomes and morphology traceable back to the primary tumor https://pubmed.ncbi.nlm.nih.gov/31162796/
Hammarsten P, Immunoreactivity for prostate specific antigen and Ki67 differentiates subgroups of prostate cancer related to outcome https://pubmed.ncbi.nlm.nih.gov/30980038/
Lindgren Belal S, Applications of Artificial Intelligence in PSMA PET/CT for Prostate Cancer Imaging https://pubmed.ncbi.nlm.nih.gov/37357026/
Trägårdh E, Freely Available, Fully Automated AI-Based Analysis of Primary Tumour and Metastases of Prostate Cancer in Whole-Body [18F]-PSMA-1007 PET-CT https://pubmed.ncbi.nlm.nih.gov/36140502/
Björeland U, Impact of neoadjuvant androgen deprivation therapy on magnetic resonance imaging features in prostate cancer before radiotherapy https://pubmed.ncbi.nlm.nih.gov/33898790/
Sandgren K, Registration of histopathology to magnetic resonance imaging of prostate cancer https://pubmed.ncbi.nlm.nih.gov/34258403/
Chappidi, Transcriptomic Heterogeneity of Expansile Cribriform and Other Gleason Pattern 4 Prostate Cancer Subtypes https://pubmed.ncbi.nlm.nih.gov/37474400/
Das R, An integrated functional and clinical genomics approach reveals genes driving aggressive metastatic prostate cancer https://pubmed.ncbi.nlm.nih.gov/34326322/
Helzer KT Fragmentomic analysis of circulating tumor DNA-targeted cancer panels https://pubmed.ncbi.nlm.nih.gov/37330052/
de Jong AC, Predicting response to enzalutamide and abiraterone in metastatic prostate cancer using whole-omics machine learning https://pubmed.ncbi.nlm.nih.gov/37031196/
ADVISORY BOARD
Prof. N James (ICR, London, PI of STAMPEDE)
Prof. D Larsson (GU, Head of Clinical Trials Sweden)
E Hallersjö Hult (Vision Zero Cancer)
Prof. P Cornford (UK, EAU Guidelines)
H Joelsson (Patient representative, prostatacancerförbundet)
R Rosenquist Brandell (GMS)
E Axén (NPCR registry)
Sven Löffeler (siv.no)

I Acta Oncologicas specialnummer om precisionsmedicin presenteras studien som ett Letter.

Regeringen har beslutat att ge 12 miljoner genom Socialstyrelen till SPRINTR-studien.

En elektronisk samtyckeslösning för forskningspersoner utvecklad vid Umeå universitet.

Forskare och projektmedlemmar från hela landet, från Luleå i norr till Lund i söder, möttes i Stockholm.

Forskning för precisionsbehandling av prostatacancer

Patientnytta och forskning i framkant – SPRINTR når 100 i Umeå!